

Α-FeOOH,呈黃色,被稱為氧化鐵黃(簡稱鐵黃),鐵黃形貌多為針狀結構,具有較好的遮蓋力、耐光性、耐候性、耐酸堿性以及吸收紫外光線等優點,被廣泛的應用于皮革、透明塑料、閃光涂料、油墨、顏料等方面,除此之外在精細陶瓷,催化劑以及生物工程領域也有良好的應用前景。
由于氧化鐵黃在177℃以上時,將會失去結合水并轉化為氧化鐵紅,為了提高氧化鐵黃的耐熱性,通常采用表面改性技術,使氧化鐵黃在高溫下保持良好的穩定性。不同的改性方法,使氧化鐵黃的表面帶電性發生改變。
Zeta電位是顆粒表面化學的體現,依賴于顆粒表面的化學組成和周圍溶液環境,不同的pH下,體現的Zeta電位不同。環境pH對于Zeta電位的影響是多種因素共同作用的結果,首先,pH的改變影響顆粒表面基團的離解平衡;其次,溶液環境中[H]+和[OH]-離子濃度不同,會影響這兩種離子在顆粒表面的吸附效果;滴定過程中加入酸或者堿不但會改變環境的pH還同時改變環境的離子強度。在解釋滴定曲線的時候需要綜合考慮這些影響因素。

圖 | BeNano 180 Zeta Pro與 BAT-1自動滴定儀
樣品制備和測試條件
將氧化鐵黃粉末分散在純凈水中得到母液,水域超聲5分鐘使其分散。檢測其pH為5.8,初始Zeta電位為正值。通過BeNano主機和BAT-1自動滴定儀進行pH滴定操作,向溶液中滴加NaOH水溶液改變體系的pH。終點pH設定為12,pH間隔為1,冗余度0.2pH值。
通過BeNano內置的溫度控制系統開機默認測試溫度控制為25℃±0.1℃,采用毛細管電極進行測試。每一個樣品在放入樣品池后進行一次測試。
測試結果和討論
通過檢測不同pH下樣品的Zeta電位值,我們得到Zeta電位隨pH的變化曲線。
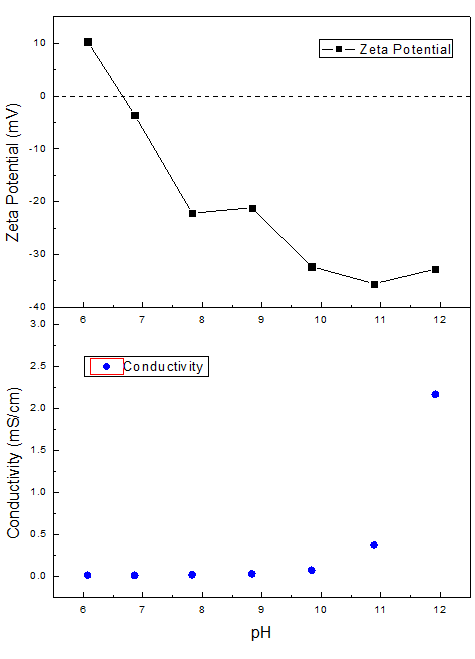
圖 | Zeta電位(上圖)和電導率(下圖)對于pH的依賴性曲線
從圖中可以看出,氧化鐵黃樣品在低pH范圍時Zeta電位為正值,說明其顆粒物上帶有較多正電,隨著pH升高,Zeta電位逐漸向0趨近,在pH=6.66時達到等電點,此時Zeta電位值為0。隨著pH繼續升高,[OH]-濃度升高,顆粒開始攜帶負電荷,其Zeta電位隨pH升高絕對值逐漸增大。
相對較高的pH(10~12)范圍(顆粒攜帶較多負電)懸浮液的Zeta電位絕對值比較高,說明體系在此范圍內相對比較穩定,不容易團聚,而在等電點附近Zeta電位較低,體系的穩定性相對較差。
當pH達到11之后,顆粒表面的負電荷基本達到飽和,即使pH繼續升高,顆粒表面也無法攜帶更多負電荷。此時繼續加入NaOH溶液在pH升高的同時,離子強度也逐漸升高。在顆粒表面電荷基本飽和的情況下,Zeta電位絕對值不再變高,而且隨離子強度加大,電導率迅速上升,屏蔽效應逐漸增加,Zeta電位絕對值有緩緩變小的趨勢。
結論
通過百特BeNano納米粒度及Zeta電位儀和BAT-1自動滴定儀表征了一個氧化鐵黃樣品在不同pH條件下的Zeta電位信息。結果表明,氧化鐵黃在pH=6.66時,為其體系的等電點,在等電點附近Zeta電位絕對值相對較低,體系處于不穩定狀態。而當較高(pH=10~12)時其體系的Zeta電位絕對值較高,處于相對穩定狀態。